
1. Overview
산염기 장애를 접근하는 3가지 주요 방식
- 1) physiological approach
- 2) base-excess approach
- 3) physiochemical approach (Stewart method)
–> 본 review 는 physiological method 를 순서대로 살펴보았다.
physiological method 의 경우 carbonic acid-bicarbonate buffer system 을 이용한다. 이러한 관점에서 CO2 의 부분압의 변화는 반응에 따른 이차적인 bicarbonate 농도 변화 적응을 유발한다. (그 반대도 성립한다.) 수소 이온의 농도는 실제적으로 대부분의 단백질과 세포막의 기능을 변화시킬 수 있으므로, 체내에서 엄밀하게 조절된다. 수소 이온은 plasma 내에서 정상적으로 매우 낮은데, (대략 40 nmol/L) 그러므로, pH 단위가 사용 된다. acidemia 나 alkalemia 라는 용어는 혈액의 pH 가 비정상적으로 낮거나, 높은 것을 지칭한다. (acidic, alkaline) 수소이온의 농도가 증가되는 것을 acidosis 라고하고, 감소하는 것을 alkalosis 라고 한다.
전통적으로 acid-base 값은 Henderson–Hasselbalch equation 에 기초하고 있다.
pH = pK + log10 (bicarbonate [HCO3−] ÷ [0.03 × partial pressure of arterial carbon dioxide (Paco2)])
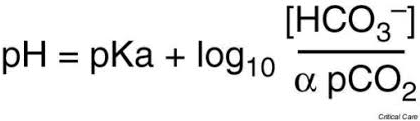
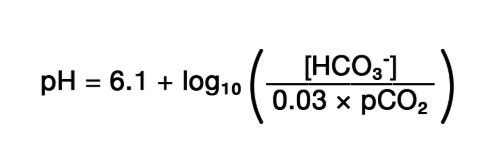
여기서 bicarbonate 단위는 mmol/L 이며, PaCO2 의 단위는 mmHg 이다. 산염기 장애가 일차적으로 respiratory function 에 의해 PaCO2 가 변하여 발생한 것이라면 respiratory 라고 하며, 일차적으로 bicarbonate 농도의 변화로 발생된 것이라면 metabolic 이라고 한다.
2. History and Physical examination
산염기 장애를 접근하는 첫번째 단계는 신중한 임상적 평가이다. (여러가지 증상, 질환, 약물 등)
활력 징후(쇼크나 패혈증을 시사할 수 있음), 신경학적 상태(의식 있음 vs. 의식 없음), 감염의 징후(예: 발열), 폐 상태(호흡수, 쿠스마울 호흡의 존재 여부, 청색증 및 손가락 곤봉 모양의 존재 여부), 위장관 증상(구토 및 설사) 등을 확인해야 합니다. 임신, 당뇨병, 심장, 폐, 간, 신장 질환 등 특정 기저 질환이 원인에 대한 단서를 제공할 수 있습니다.
임상의는 환자가 산-염기 균형에 영향을 미치는 약물(예: 완하제, 이뇨제, 토피라메이트, 메트포르민 등)을 복용했는지를 확인해야 하며, 산-염기 장애와 관련된 중독의 징후를 고려해야 합니다. 예를 들어, 아세톤 냄새는 당뇨병성 케톤산증 또는 이소프로필 알코올 중독의 신호일 수 있고, 시야 장애는 메탄올 중독의 증상일 수 있습니다.
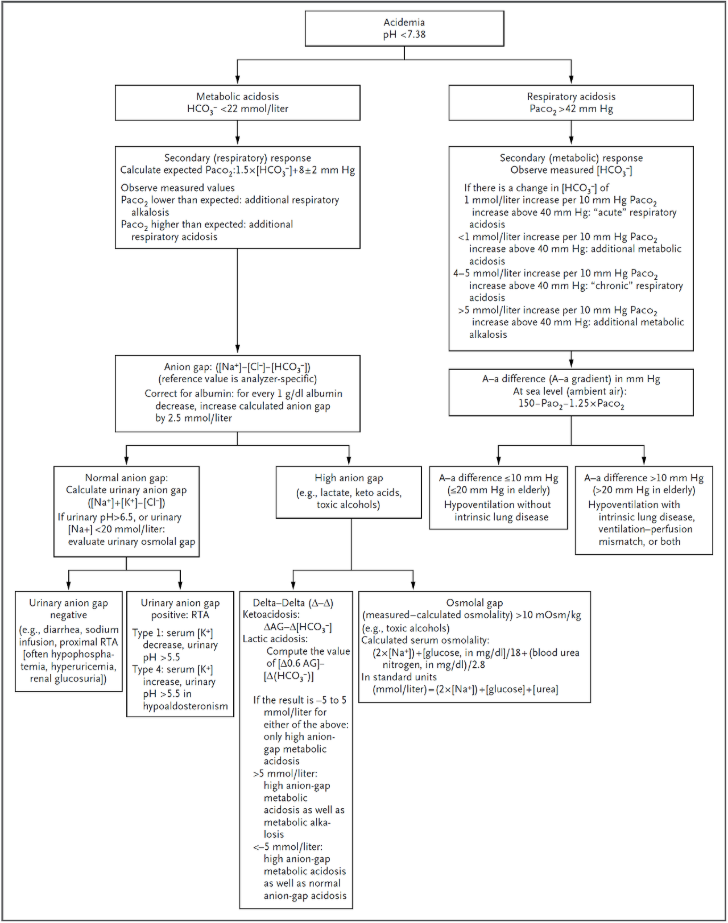
3. Determination of the primary acid-base disorder and the secondary response
두번째 단계는 일차적인 산염기 장애가 무엇인지 파악하고, 그에 대한 이차적인 반응을 살펴보는 것이다. 생명이 있는 상태에서 가능한 pH 의 범위는 7.8~6.8 이다. (수소 이온의 농도로는 16~160 nm/L) pH 의 reference value 는 7.40±0.02, Paco2 의 경우는 38±2 mm Hg [HCO3−] 의 경우 24±2 mmol per liter 이다. (본 리뷰에서 사용) 이러한 4가지 항목들의 변화가 primary acid-base disorder 를 결정하게 된다.
경험적으로 산염기 변화에 반응하여 항상성을 유지하기위한 반응들을 예측할 수 있고 계산해 볼 수 있다. 대사성 산염기 변화의 경우 호흡수가 급격히 변하여 수시간내에 새로운 PaCO2 평형 상태를 형성한다. 한편 호흡이 만성적으로 비정상적이어서 발생하는 대사성 보상은 천천히 발생하여 혈청 bicarbonate 의 농도가 새로운 평형 상태를 형성하기 위해서 2~5일 정도가 소요된다. 따라서 bicarbonate 농도가 특정 기준을 만족하는지에 따라 호흡 변화가 acute 인지 chronic 인지 알 수 있다.

하지만 여기서 몇가지 함정이 있다. 혈액 가스 수치는 항상 2가지 이상의 함께 존재하는 산염기 질환으로 설명될 수 있으며, 현재 산염기의 질환의 반응을 예측하는 공식은 거의 40년전에 사람과 개를 대상으로 연구된 자료들이라는 점이다. 따라서 특정한 경우에는 예측이 들어맞지 않을 수 있다.
4. Evaluation of the metabolic component of an acid-base disorder
세번째 단계는 산염기 질환의 metabolic component 를 고려하는 것이다.
1) Metabolic acidosis
metabolic acidosis 를 평가하는 초기 단계는 anion gap 을 계산해보는 것이다.
[Na+] + [K+] + [Ca2+] + [Mg2+] + [H+] + unmeasured cations = [Cl−] + [HCO3−] + [CO32−] + [OH−] + albumin + phosphate+ sulfate + lactate + unmeasured anions (e.g., inorganic anions)
이러한 이온들을 다 측정하는 것은 불필요하므로, 실제적으로는 혈액내 가장 많은 3가지 이온으로 계산한다.
Anion gap = [Na+]−[Cl−] − [HCO3−]
(reference ranges of 3.0 to 12.0 mmol per liter up to 8.5 to 15.0 mmol per liter in the anion gap have been reported)
(1) High-anion-Gap metabolic acidosis
GOLD MARRK 라고 외우면 편하다.
- G : glycols [ethylene and propylene]
- O : 5-oxoproline [pyroglutamic acid]
- L : l-lactate
- D : d-lactate
- M : methanol
- A : aspirin
- R : renal failure
- R : rhabdomyolysis
- K : ketoacidosis
Anion gap 은 Na 와 Cl 이온에 비해 상대적으로 bicarbonate 가 감소하여 증가한다.
- acid 의 과생성으로 인해 bicarbonate 가 감소하는 경우 : in ketoacidosis, lactic acidosis, and drug and alcohol-related intoxication
- 산의 배출이 안되어 bicarbonate 가 감소하는 경우 : in advanced renal failure
- Cell lysis 로 인해 bicarbonate 가 감소하는 경우 : in massive rhabdomyolysis
- 기타 다른 상황 : e.g., the use of penicillin-derived antibiotics
(2) Uses and Limitation of the Anion Gap
lactic acidosis 의 경우 high anion gap metabolic acidosis 의 반 이상을 차지하는데, 대게의 경우 shock 이나 tissue hypoxia 로 인해 발생한다. 하지만 anion gap 은 상대적으로 반영이 안되는데, lactate level 이 3.0~5.0 mmol/L 인 환자들 중 대략 반수 이상의 환자들이 anion gap 이 정상이었다. 즉 lactate 상승에 대해 anion gap 은 sensitivity 와 specificity 가 모두 80% 아래여서 serum lactate level 을 대체할 수 없다.
또한 anion gap 은 항상 albumin 수치에 따라 보정을 해야하는데, albumin 은 약산성 물질로서 anion gap 의 75% 를 차지하고있기 때문이다. hypoalbuminemia 에서 보정을 하지 않았을 경우 anion gap 은 약 50% 이상에서 5이상으로 증가되지 않았다. serum albumin 보정은 1g/dL 감소시마다 anion gap 을 2.3~2.5 mmol/L 더해서 계산해야 한다.
anion gap 은 diabetic ketoacidosis 를 진단하는데 도움을 주며, 이러한 상황에서 ketosis 가 호전되는지 추적할 수 있게 해준다. 또한 이러한 환자에서 많은 양의 생리식염수를 주입했다면 normal anion-gap acidosis 를 확인할 수 있다.
high anion gap 이면서 normal lactate level 인 알코올 중독 환자의 경우 alcoholic ketoacidosis 진단의 중요한 단서가 된다. alcoholic ketoacidosis 의 경우 ketouria 가 없다고 해서 잘못 해석되기도 한다. )일차적으로 생성되는 beta-hydroxybutyrate 의 경우 소변검사의 nitroprusside test 로는 검출이 되지 않기 때문이다. acetoactate 만 검출이 된다.) 또한 pH 가 정상이거나 상승이 되어있기도 하는데, 그 이유는 vomiting 으로 인한 metabolic alkalosis 가 혼재되어 있거나, liver disease, Pregnancy, high temperature 또는 sepsis 로 respiratory alkalosis 가 병발되었기 때문이다.
또한 anion Gap 은 D-lactic acidosis 를 진단하는데 도움을 준다. (short-bowel syndrome : 이 경우 standard lactate level (L-lactate) 는 정상인 반면, anion gap 은 상승되어 있다.)
hyperchloremia 일 때 anion gap 이 매우 낮거나 negative 인 경우가 발생한다. hyperchloremia 의 경우 lithium toxicity 나 monoclonal IgG gammopathy 혹은 high Ca 또는 Mg 인 질환에서 발생한다. 또한 bromide 또는 iodide intoxication 에서 pseudohyperchloremia 가 발생하여 원인이 되기도 한다.
* 참고 : L-lactate, D-lactate
두 가지 젖산 이성질체는 L-젖산(L-lactate)과 D-젖산(D-lactate)으로 알려져 있으며, L-젖산은 (+) 방향으로, D-젖산은 (–) 방향으로 편광된 빛을 회전시킵니다. 이러한 성질은 때때로 사용되는 명명법인 D(–)-젖산과 L(+)-젖산에 반영되어 있습니다. 두 형태의 젖산(입체이성질체)은 모두 젖산탈수소효소(LDH)의 작용을 통해 피루브산으로부터 생성되거나 피루브산으로 대사될 수 있습니다. 그러나 이 효소는 이성질체 특이성을 가지고 있어, D-젖산의 생성과 대사에는 D-LDH가 필요하고, L-젖산의 생성과 대사에는 L-LDH가 필요합니다. 포유류 세포는 L-LDH만을 보유하고 있기 때문에 인간에서 생성되는 젖산은 거의 전적으로 L-젖산입니다. 반면, 탄수화물을 발효하는 일부 박테리아(예: 유산균종)는 두 효소를 모두 가지고 있어 D-젖산과 L-젖산을 모두 생성할 수 있습니다. 일부 종은 D-젖산만을, 일부는 L-젖산만을, 또 다른 종은 두 형태 모두를 생성합니다.
요약하면, 정상적으로 혈액 내에서 소량 존재하는 D-젖산은 다음의 세 가지 경로로부터 유래합니다:
- 메틸글옥살 경로를 통한 세포 내 생산
- D-젖산이 함유된 식이(예: 요거트, 사워크림, 치즈 등)
- 대장에서 정상적으로 서식하는 젖산 생성 박테리아 종
D-젖산 농도의 유의미한 증가로 인해 산증이 발생할 수 있는 유일한 병태는 단장 증후군(short-bowel syndrome)으로, 이 상태는 대장에서의 박테리아 과증식이 특징입니다.
단장 증후군에서 D-젖산산증이 발생하는 주요 병태 생리는 탄수화물 흡수 장애입니다. 외과적 장 절제로 인해 소장에서 정상적으로 일어나야 할 탄수화물의 소화 및 흡수 능력이 감소하고, 이에 따라 많은 양의 탄수화물이 대장으로 전달되며, 이곳에는 탄수화물을 발효하는 박테리아가 서식하고 있습니다.
대장에서 박테리아는 유입된 탄수화물을 젖산으로 전환하며, 이때 D 및 L 이성질체가 모두 생성됩니다. 이들 젖산은 대장에서 흡수됩니다. 체내는 L-LDH를 통해 비정상적으로 증가한 L-젖산의 처리에 충분한 대사 능력을 갖고 있지만, D-젖산의 경우 대사 능력이 매우 제한적입니다. 이 처리 능력을 초과하게 되면 혈중 D-젖산이 축적되고, 궁극적으로 D-젖산산증이 발생하게 됩니다.
(요약하면, 사람은 L-lactate 만 있는데, 음식이나, 장내 세균 등으로 소량 D-lactate 가 있을 수는 있다. 하지만 D-lactic acidosis 는 bacterial overgrowth 인 경우 발생할 수 있는데, short bowel syndrome 에서는 carbohydrate 를 흡수를 잘 못하게 되고 장내에 많이 쌓이게되어 D-lactate 가 많이 생성된다는 설명.)
(3) Normal anion-Gap acidosis
Chloride 는 세포내, 외의 산-염기 조절에서 중요한 역할을 하는데, normal anion-gap acidosis 는 bicarbonate 이온이 감소하면서 전기적 중성을 맞추기 위해 chloride 이온이 따라서 증가하므로서 발생한다. 다른 말로는 hyperchloremic metabolic acidosis 라고도 한다. 이러한 형태의 산증은 소화기관으로의 bicarbonate 의 소실 (e.g., because of diarrhea or ureteral diversion), 신장으로의 bicarbonate loss (즉 bicarbonate 생성이 안되는 것, may occur in defective urinary acidification by the renal tubules ;renal tubular acidosis), 또는 초기 신부전에서 acid 배출이 안될 때 발생한다. 병원에서는 hyperchloremic acidosis 는 주로 생리식염수를 상당량 정주했을 때 발생하기도 한다.
Hyperchloremic acidosis 에서는 ammonium 의 소변으로의 배설이 증가되는데, 소변에서의 ammonium 이온을 측정하면 normal anion-gap acidosis 가 신장이 원인인지, 신장외 원인인지 구별할 수 있다. 하지만 소변의 ammonium 이온은 잘 측정하지 않기 때문에 urinary osmolal gap 으로 대체하여 urinary ammonium 의 배출을 평가할 수 있다.
Urinary anion gap 은 [Na+]+[K+]–[Cl−] 로 계산할 수 있으며, normal anion-gap acidosis 에서 보통 negative 를 띤다. 하지만 Urinary ammonium 이온 (NH4Cl 형태로) 의 배출이 안되는 경우 (renal failure 나 distal RTA, hypoaldosteronism 등에서) positive 가 된다.
Normal anion-gap acidosis 에서 negative urinary anion gap 은 diarrhea, Proximal RTA (distal acidification 은 유지됨.) 등에서 확인된다.
* 후려치기 –> acid 가 배출이 안되면 positive, acid 가 배출이 되면 negative urinary anion gap!
Urinary anion gap 은 polyuria 일때나, Urine pH 가 6.5 초과할 때, urinary ammonium 이 Cl 이 아닌 다른 음이온과 함께 배출될때 (Keto acids, acetylsalicylic acid, D-lactic acid, 많은 양의 penicillin 등) 는 신뢰하기 힘들다.
게다가 urine 의 acidification 은 충분한 양의 Na 의 distal delivery 가 바탕이되어야 하기 때문에, Urine Na 이 20 mmol/L 이하인 경우 urine anion gap 을 믿기 힘들다.
이러한 경우에는 Urinary osmolal gap 을 구하는 것이 도움이 된다.
Urinary osmolal gap = measured Urine Osm – calculated Urine Osm
Calculated urine osm =
(2 × [Na+] + 2 × [K+]) + (Urine Urea nitrogen[mg/dL] ÷ 2.8) + (urine glucose [mg/dL] ÷ 18)
or (2 × [Na+] + 2 × [K+]) + (urine urea nitrogen)[mmol/L] + (urine glucose)[mmol/L]
당뇨가 없는 환자의 경우 Glucose 는 보통 빼기도 한다.
Urinary Osmolal gap 이 40 mmol/L 이하이고, normal anion-gap acidosis 라면 urine ammonium excretion 이 안된다는 것을 의미한다. Urine Osm gap 은 보통 ammonium level 을 반영하기 때문이다. (많은 양의 nondissociated acid – beta hydroxybutyric acid in ketoacidosis 가 존재할 경우는 예외이다.)

2) Metabolic alkalosis
정상적인 kidney 라면 많은 양의 bicarbonate 를 배설하는 것은 어렵지 않기 때문에, metabolic alkalosis 가 발생하려면 alkali 가 많이 생성되야 하고 동시에 bicarbonate 의 신장 배설이 되지 않아야 가능하다.
위액을 소실하거나, 이뇨제를 사용하는 경우가 metabolic alkalosis 의 대표적인 경우들이다.
소변에서 Chloride 를 측정하므로써 Chloride-responsive 와 Chloride-resistant metabolic alkalosis 를 구별할 수 있다. 유효순환 volume 이 감소하였을 경우 신장은 RAAS 의 활성화를 통해 사구체에서 여과된 Na, Bicarbonate, Cl 을 재흡수한다. 따라서 소변의 Cl 의 농도는 감소하게 된다.
Spot urine chemistry 에서 Chloride 농도가 25 mmol/L 이하라면 Chloride-responseive metabolic alkalosis 를 뜻한다. NaCl 이 포함된 fluid 를 정주하므로써 (보통 KCl 과 함께.) 유효 동맥 volume 과 potassium 이 보충되며, 동시에 metabolic alkalosis 가 교정된다.
Spot urine chemistry 에서 Chloride 농도가 40 mmol/L 이상이라면 주된 원인은 신장에서 NaCl 이 부적절하게 배출되었기 때문이다. 보통 mineralocorticoid 과다 혹은 severe hypokalemia ( 2 mmol/L 미만 ) 인 상황을 반영한다. 이러한 경우 NaCl fluid 의 투여는 metabolic alkalosis 를 교정하지 못한다. 따라서 Chloride-resistant 라고 한다.
Diuretic-induced metabolic alkalosis 는 예외적으로 처음에는 소변내의 chloride 농도가 높았다가 이뇨제의 효과가 줄어들면서 Chloride 의 소변내 농도는 25 mmol/L 로 감소하게 된다.
또다른 중요한 chloride-resistant metabolic alkalosis 의 원인으로 Bartter syndrome 과 Gitelman syndrome, Extreme hypercalcemia, severe magnesium deficiency 가 있다. 이러한 원인들은 hyperaldosteronism 과는 다르게 Sodium retention 을 일으키지는 못한다. (Sodium retention –> Hypertension)
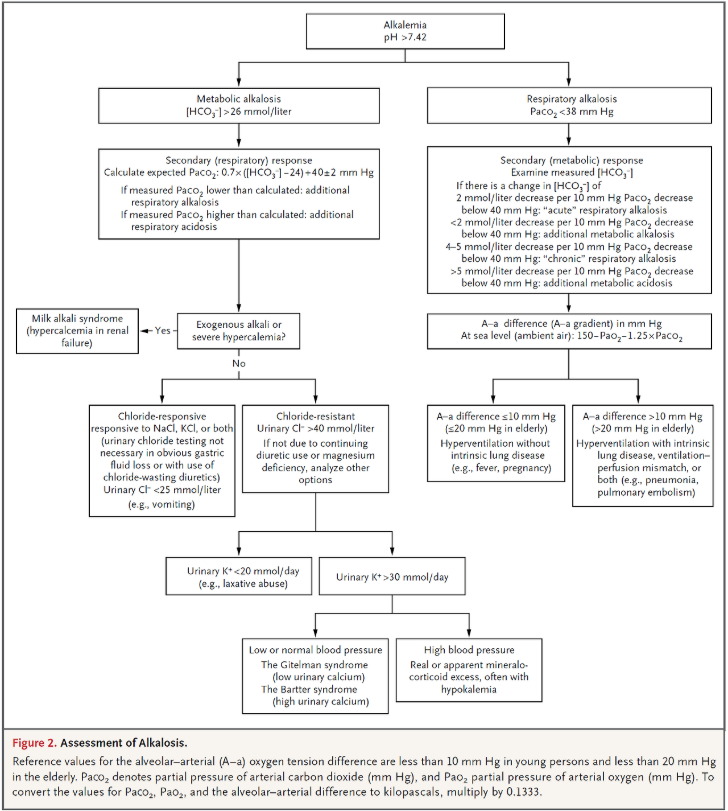
5. Evaluation for the presence of mixed metabolic acid-base disturbances
산염기 질환 평가의 4번째 단계는 mixed metabolic acid-base disturbances 의 가능성을 고려하는 것이다. high anion gap metabolic acidosis 에서 anion gap 의 크기 정도 (delta AG) 는 bicarbonate 의 감소량 (delta HCO3) 와 관련이 있다. high anion gap acidosis 와 metabolic alkalosis 혹은 normal anion gap acidosis 가 동시에 존재하는지 확인하기 위해서 delta-delta 방법이 사용된다.
delta AG 는 AG 가 12 mmol/L 에서 얼마나 더 증가했는지 그 차이를 뜻하며,
delta HCO3 는 Bicarbonate 가 24 mmol/L 에서 얼마나 더 감소했는지 그 차이를 말한다.
ketoacidosis 에서 delta AG 와 delta HCO3 의 비율은 1:1 정도이다.
lactic acidosis 에서 delta AG 와 delta HCO3 의 비율은 1:0.6 이다.
이러한 비율 차이는 아마도 lactate 가 keto-anions 에 비교해서 renal clearance 가 적기 때문에 그랬을 것으로 설명한다.
lactic acidosis 에서 delta AG 와 delta HCO3 의 비율이 1:1 이라면 very acute lactic acidosis 를 의미한다. (경련을 한 직후라던가, 운동을 하고 탈진한 시점이 그 예이다.)
만약 ketoacidosis 에서 [delta AG] – [delta HCO3] 가 +- 5 이내라면 단순히 high anion gap metabolic acidosis 이겠지만, (lactic acidosis 에서는 0.6 x [delta AG] – [delta HCO3] 의 값이) +5 mmol/L 를 초과하면 metabolic alkalosis 가 동시에 있는 것이고, -5 mmol/L 를 미만이라면 normal anion gap metabolic acidosis 가 동시에 있는 것이다.
6. Consideration of the Serum (or Plasma) Osmolal Gap
산염기 질환 평가의 5번째 단계는 설명되지 않는 high anion-gap acidosis, coma, toxic alcohol ingestion 의심, iatrogenic propylene glycol 중독의 위험이 높은 입원 환자 (e.g. 중환자실에서 high-dose lorazepam 으로 진정) 등에서 osmolal gap 을 사용하는 것이다. 예를들어 toxic alcohol ingestion 의 경우 바로 검사가 가능하지 않기 때문에, 임상의들은 이 질환을 빨리 의심해서 치료를 해야 한다.
Osmolal gap = Measured serum Osm – Calculated serum Osm
Calculated serum Osm = 2 × (Na+[mmol/L]) +(glucose[mg/dL]) ÷ 18 + (BUN[mg/dL]) ÷ 2.8
만일 ethanol 을 포함하여 계산하려면 Ethanol 의 양 (mg/dL) 을 3.7 로 나누면 된다.
Osmolal gap 이 +- 10 mOsm/kg 이내면 정상이나, +- 10 을 초과하면 비정상이다.
Osmolal gap 의 한계로는 ethylene glycol 이나 methanol intoxication 뿐만 아니라 lactic acidosis, alcoholic ketoacidosis, diabetic ketoacidosis 에서도 증가할 수 있다는 점이다.
7. Evaluation of the respiratory component of an acid-base disorder
산염기 질환의 호흡기적 요소는 acute 와 chronic 으로 나눌 수 있다. hypoxemia 의 경우 lactic acidosis 의 주된 원인이되며, respiratory alkalosis 를 유도할 수 있다. Ventilation 에 대한 상대적인 PaO2 를 평가하기 위해서 alveolar-arterial Oxygen-tension difference (AaDO2) 를 사용할 수 있으며, 폐질환으로 인한 것인지, 폐외 질환으로 인한 것인지 구분할 수 있게 한다. 환자가 폐 질환이 있는 경우 AaDO2 (alveolar 의 PAO2 와 alveolar-capillary membrane 의 arterial side 의 PaO2 의 차이) 가 클 것이다. 정상적으로 젊은 사람의 경우 AaDO2 는 5~10 mmHg 미만이며, 건강한 노인의 경우 15~20 mmHg 미만이 된다.
AaDO2 = Fio2 × (barometric pressure – water-vapor pressure) – Pao2 – (Paco2 ÷ gas-exchange ratio)
대기중에서 FiO2는 0.21 이 되며, Barometric pressure 는 해수면에서 760 mmHg 가 된다. water-vapor pressure 는 37도씨에서 47 mmHg 가 된다. Gas exchange ratio 는 평형상태에서 약 0.8 정도가 된다.
따라서 대기중에, 해수면에서, 37도씨 체내에서 AaDO2 는 다음의 식으로 요약할 수 있다.
Fio2 × (760 − 47) − Pao2 − (Paco2 ÷ 0.8)
= 150 – Pao2 − 1.25 Paco2
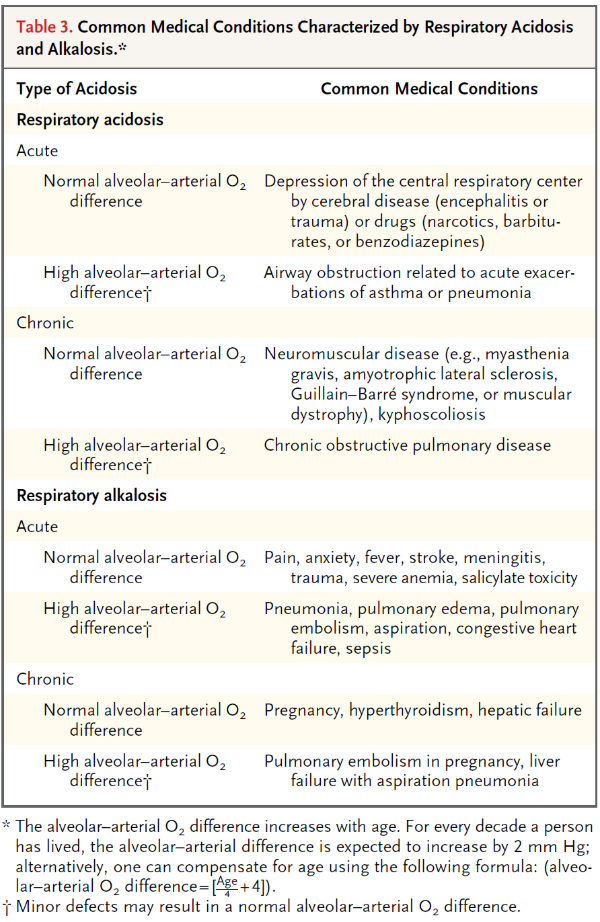
8. Interpretation of Acid-base disorders in the clinical context
산염기 질환 평가의 마지막 단계는 cause of the identified processes 를 결정짓는 것이다.